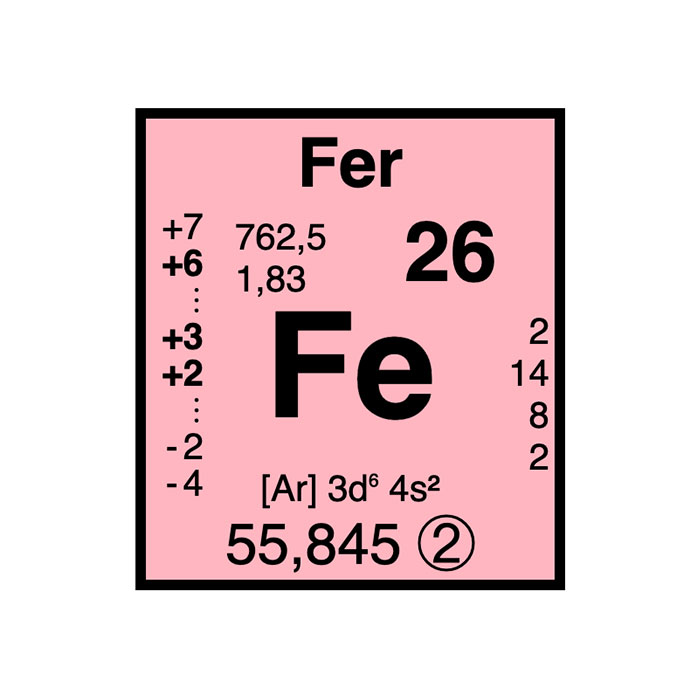
Caractéristiques du fer
- Symbole : Fe
- Masse atomique : 55,845 ± 0,002 u
- Numéro CAS : 7439-89-6
- Configuration électronique : [Ar]4s23d6
- Numéro atomique : 26
- Groupe : 8
- Bloc : Bloc D
- Famille d’éléments : Métal de transition
- Électronégativité : 1,96
- Point de fusion : 1 538 °C



