Pouvant être synthétisé par l’organisme, l’aspartate est reconnu pour ses rôles biologiques importants. En plus de sa capacité à stimuler les hormones sexuelles, il intervient dans la gluconéogenèse et dans la constitution des protéines. Cet acide aminé est présent dans de nombreux aliments.
Description de l’aspartate
L’acide aspartique est une poudre sèche de couleur blanche, présentant un goût acide. Il se forme naturellement dans le corps à partir de l’oxaloacétate, grâce à une réaction de transamination catalysée par l’enzyme aminotransférase. Ce processus implique le transfert d’un groupe amine provenant de l’alanine ou de la glutamine en vue de former de l’alpha-cétoacide et de l’aspartate.
Il est aussi possible de synthétiser chimiquement l’acide aspartique à partir de phtalimidomalonate de diéthyle. Cependant, cette méthode permet d’obtenir l’acide DL-aspartique, qui dispose de fonctions biologiques limitées. Désormais, les techniques adoptées en biotechnologie, mettant en œuvre des enzymes immobilisées, permettent de former l’une des deux énantiomères de manière plus ciblée.
Histoire de l’aspartate
En 1827, Auguste-Arthur Plisson, un chimiste d’origine française, a identifié l’aspartate. Le nom de ce dernier a été dérivé de l’asparagine, la substance utilisée pour l’isoler. Il s’agit d’un autre acide aminé qui a été découvert dans le jus extrait d’asperge en 1806.
Structure de l’aspartate
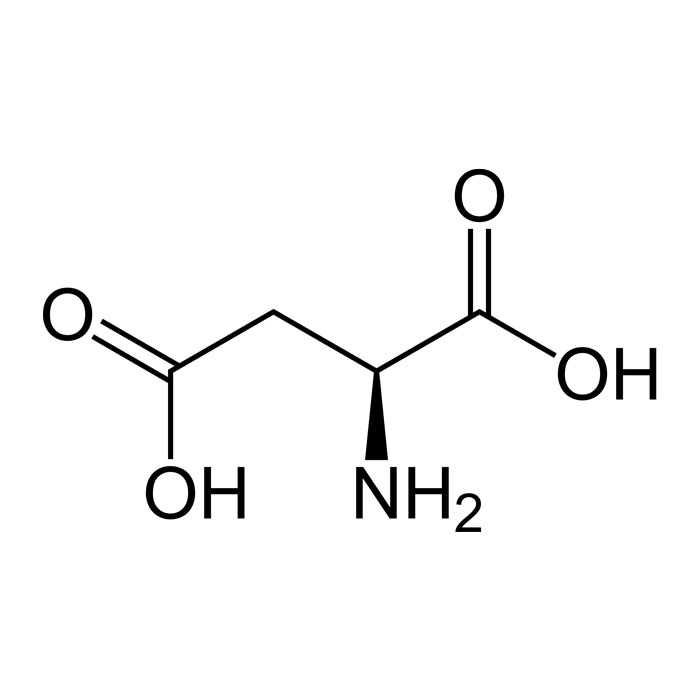
L’acide aspartique présente deux groupements fonctionnels, à savoir un groupe amine (NH2) et un groupe carboxyle (COOH). Sa chaîne latérale est représentée par -CH2-COOH. Il se distingue par la présence d’une seconde fonction carboxyle. Cette particularité en fait un acide aminé polaire et dicarboxylique, le rendant ainsi l’élément le plus acide parmi les constituants des protéines.
Fonctions physiologiques de l’aspartate
L’aspartate joue de rôles importants dans l’organisme. Il intervient dans de nombreux processus biologiques.
La gluconéogenèse
L’acide aspartique participe au processus de gluconéogenèse. Il s’agit d’une série de réactions biochimiques visant à synthétiser du glucose et à maintenir le taux sanguin à des niveaux normaux. L’aspartate transfère son groupe amine à l’α-cétoglutarate, déclenchant ainsi une réaction qui conduit à la production de l’oxaloacétate. Ce dernier est ensuite converti en acide phosphoénolpyruvique. Par la suite, la néoglucogenèse emprunte la voie opposée de la glycolyse. De son côté, l’α-cétoglutarate est transformé en L-glutamate.
La biosynthèse de pyrimidines
L’aspartate contribue à la biosynthèse de pyrimidines, des molécules azotées hétérocycliques indispensables à la création des nucléotides pyrimidiques. Ces derniers sont les éléments de base des molécules d’ARN et d’ADN.
Le cycle de Krebs
En tant que précurseur de l’oxaloacétate, l’acide aspartique joue un rôle majeur dans le cycle de Krebs.
L’activation des récepteurs ionotropes NMDA
L’aspartate active les récepteurs NMDA, une action présentant des implications importantes. Elle facilite l’entrée du potassium, du calcium et du sodium dans les neurones. Cette stimulation contribue également à la synthèse de la gonadolibérine. Sécrétée par l’hypothalamus, cette dernière régule la libération de FSH et de LH par l’hypophyse.